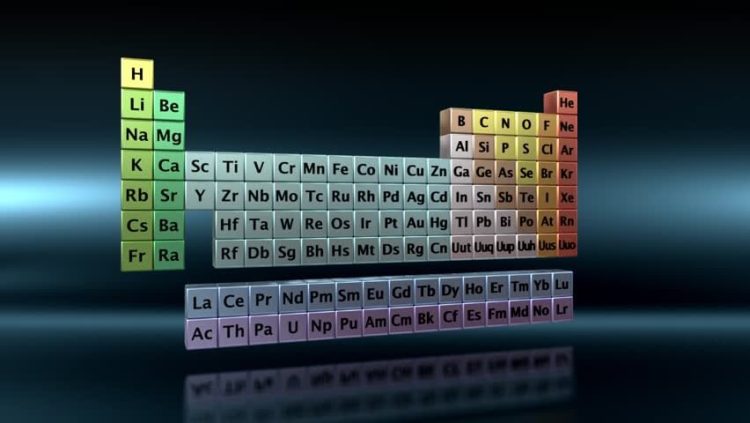
Tabel periodik unsur adalah alat yang sangat penting dalam dunia kimia. Ini adalah pengaturan sistematis dari semua unsur kimia yang diketahui berdasarkan nomor atom, konfigurasi elektron, dan sifat kimia mereka.
Dalam artikel ini, sobat akan mempelajari unsur-unsur apa saja yang ada dalam tabel periodik, termasuk karakteristik utama dan kegunaannya.
Pengertian Tabel Periodik
Tabel periodik pertama kali dibuat oleh Dmitri Mendeleev pada tahun 1869. Mendeleev menyusun unsur-unsur berdasarkan massa atom, tetapi saat ini unsur-unsur disusun berdasarkan nomor atom (jumlah proton dalam inti atom).
Tabel ini terbagi menjadi beberapa periode (baris horizontal) dan golongan (kolom vertikal), yang membantu dalam mengelompokkan unsur-unsur dengan sifat kimia yang serupa.
Golongan Utama dalam Tabel Periodik
- Golongan Alkali (Golongan 1):
- Unsur: Litium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Cesium (Cs), Francium (Fr)
- Karakteristik: Sangat reaktif, terutama dengan air; memiliki satu elektron valensi.
- Kegunaan: Litium digunakan dalam baterai, natrium dalam garam meja, dan kalium dalam pupuk.
- Golongan Alkali Tanah (Golongan 2):
- Unsur: Berilium (Be), Magnesium (Mg), Kalsium (Ca), Stronsium (Sr), Barium (Ba), Radium (Ra)
- Karakteristik: Kurang reaktif dibandingkan alkali, tetapi masih cukup reaktif; memiliki dua elektron valensi.
- Kegunaan: Magnesium digunakan dalam paduan logam ringan, kalsium dalam produk susu, dan barium dalam radiologi medis.
- Golongan Halogen (Golongan 17):
- Unsur: Fluor (F), Klor (Cl), Brom (Br), Iodin (I), Astatin (At), Tennessine (Ts)
- Karakteristik: Sangat reaktif, terutama dengan logam alkali dan alkali tanah; memiliki tujuh elektron valensi.
- Kegunaan: Klor digunakan dalam desinfeksi air, fluor dalam pasta gigi, dan iodin dalam antiseptik.
- Golongan Gas Mulia (Golongan 18):
- Unsur: Helium (He), Neon (Ne), Argon (Ar), Kripton (Kr), Xenon (Xe), Radon (Rn), Oganesson (Og)
- Karakteristik: Tidak reaktif (inert) karena memiliki konfigurasi elektron yang stabil; memiliki delapan elektron valensi (kecuali helium yang memiliki dua).
- Kegunaan: Helium digunakan dalam balon dan pendingin kriogenik, neon dalam lampu neon, dan argon dalam pengelasan.
Unsur Transisi
Unsur-unsur ini terletak di tengah tabel periodik (Golongan 3-12). Mereka memiliki karakteristik berikut:
- Karakteristik: Dapat membentuk berbagai bilangan oksidasi dan memiliki sifat logam seperti kekerasan, konduktivitas listrik, dan daya tahan.
- Kegunaan: Besi (Fe) dalam pembuatan baja, tembaga (Cu) dalam kabel listrik, dan emas (Au) dalam perhiasan.
Kegunaan Tabel Periodik
Tabel periodik tidak hanya berguna dalam bidang kimia, tetapi juga dalam fisika, biologi, teknik, dan berbagai ilmu terapan lainnya. Dengan mengetahui posisi suatu unsur dalam tabel periodik, sobat bisa memprediksi sifat-sifat kimianya, reaktivitasnya, dan cara penggunaannya dalam kehidupan sehari-hari maupun industri.
Tabel periodik adalah alat yang sangat penting dan bermanfaat dalam ilmu pengetahuan. Dengan memahami unsur-unsur yang ada di dalamnya, sobat dapat lebih memahami sifat kimia dan fisika dari setiap unsur.
Bagi sobat yang ingin mempelajari tabel periodik dengan lebih mudah, silahkan unduh aplikasi Tabel Periodik Unsur Kimia dari Satu Nusa Aplikasi melalui smartphone. Aplikasi tersebut memuat 118 unsur kimia lengkap beserta keterangannya dalam bahasa Indonesia. Tunggu apalagi? Yuk, unduh sekarang juga!